01.08.2022 Viszeralchirurgie
Update Leberchirurgie
CHIRURGIE
Update Leberchirurgie
Die Leberchirurgie ist zentraler Eckpfeiler in der Therapie primärer Lebertumore und hepatisch metastasierter Tumorerkrankungen [1] – mit verbesserter medizinischer Evidenz und zunehmender Patientensicherheit erfolgt heute eine immer breitere Indikationsstellung zur Leberresektion. Dies basiert sowohl auf der Implementierung technischer Innovationen als auch der kontinuierlichen Verbesserung perioperativer Behandlungskonzepte. Wichtige Neuerungen der letzten Jahre liegen in der Einführung spezifischer Maßnahmen zur Reduktion von perioperativen Komplikationen und zur Verbesserung des Outcomes [2]. Dies ist von besonderer Bedeutung im Rahmen von multimodalen Therapiekonzepten, bei denen die Leberresektion nur ein Teil des onkologischen Behandlungspfades darstellt und Folgetherapien ohne Verzögerung erfolgen sollen.
Die Einführung minimalinvasiver Operationsverfahren stellt einen weiteren relevanten Entwicklungsschritt in der modernen Leberchirurgie dar: So zeigen die letzten Jahre einen deutlichen Trend zur Implementierung der robotisch-assistierten Leberchirurgie, welche eine konsequente Weiterentwicklung der laparoskopischen Leberchirurgie darstellt und Vorteile dieses Verfahrens mit der technischen Innovation des Operationsroboters kombiniert. In diesem Beitrag sollen diese Themen beleuchtet werden und so ein kurzes Update über die aus unserer Sicht für die Leberchirurgie entscheidenden Entwicklungsschritte der letzten Jahre gegeben werden.
Perioperatives Management
Perioperative Konzepte zur Verbesserung des Outcomes nach spezifischen Eingriffen (Stichwort Fasttrack) waren schon länger in der Chirurgie bekannt, nichtsdestotrotz stellt die konsequente Umsetzung solcher Konzepte in die klinische Praxis eine fortwährende Herausforderung dar. Schon innerhalb chirurgischer Subspezialisierungen, wie zum Beispiel der Viszeralchirurgie, ist ein für alle Patienten gültiger Behandlungspfad bzw. einer Standardlösung aufgrund der Komplexität der Krankheitsbilder und der Behandlungskonzepte nicht umsetzbar. In der klinischen Praxis einer viszeralchirurgischen Station bedeutet dies beispielsweise, dass Patienten nach einer minimalinvasiven atypischen Leberresektion schneller mobilisiert und Kost aufgebaut werden als nach einer offenen Trisektorektomie. Dieser Umstand wird durch die im Jahr 2016 von der ERAS-Gesellschaft (Enhanced Recovery After Surgery) publizierten Leitlinien für die perioperative Versorgung in der Leberchirurgie adressiert [3]. Durch 23 spezifische Maßnahmen (Items) wird dabei das prä-, intra- und postoperative Management spezifiziert, um so die Komplikationsraten zu reduzieren.
An der Chirurgischen Klinik der Charité wurden diese Leitlinien in einer prospektiven Observationsstudie mit 304 konsekutiv eingeschlossenen Patienten validiert [4]. Die Rate an Gesamtkomplikationen zeigte einen signifikanten Rückgang von 41,2 % (n=21) in der Nicht-ERAS-Gruppe auf 26,5 % (n=67) in der ERAS-Gruppe (P=0,0423). Dies war hauptsächlich auf den Rückgang der Clavien-Dindo Komplikationen des Grades 1-2 von 17,6 % (n=9) auf 7,6 % (n=19) zurückzuführen (P=0,0322). Dieser Effekt war sowohl nach offener als auch nach minimalinvasiver Leberresektion zu beobachten. Entscheidend bei der Implementierung eines solchen Programmes ist die Einbeziehung der Anästhesie, der Intensivmedizin und der Pflege. Durch die Bildung eines Kernteams werden Standardarbeitsanweisungen (engl. Standard operating procedures) erarbeitet und Patienteninformationsbroschüren sowie Patiententagebücher erstellt, die zu einer stringenten Umsetzung der Maßnahmen in den verschiedenen perioperativen Phase beitragen sollen.
Das Monitoring bzw. die Umsetzungskontrolle dieser Maßnahmen erfolgt über die sogenannte Adherence, welche in einer Datenbank erfasst wird. So kann beispielsweise nachvollzogen werden, ob die Mobilisierung erfolgreich umgesetzt wurde, [5], und es können (ungewollte) Veränderungen in den postoperativen Abläufen erkannt werden. Die einzelnen ERAS-items werden so ständig validiert und können angepasst werden. Bei Bedarf kann das Klinikpersonal entsprechend nachgeschult werden, um die Umsetzung der Maßnahmen zu verbessern. Die Kosten eines solches Programmes sind nicht unerheblich, wenngleich diese über eine geringere postoperative Komplikationsrate amortisiert werden können [2].
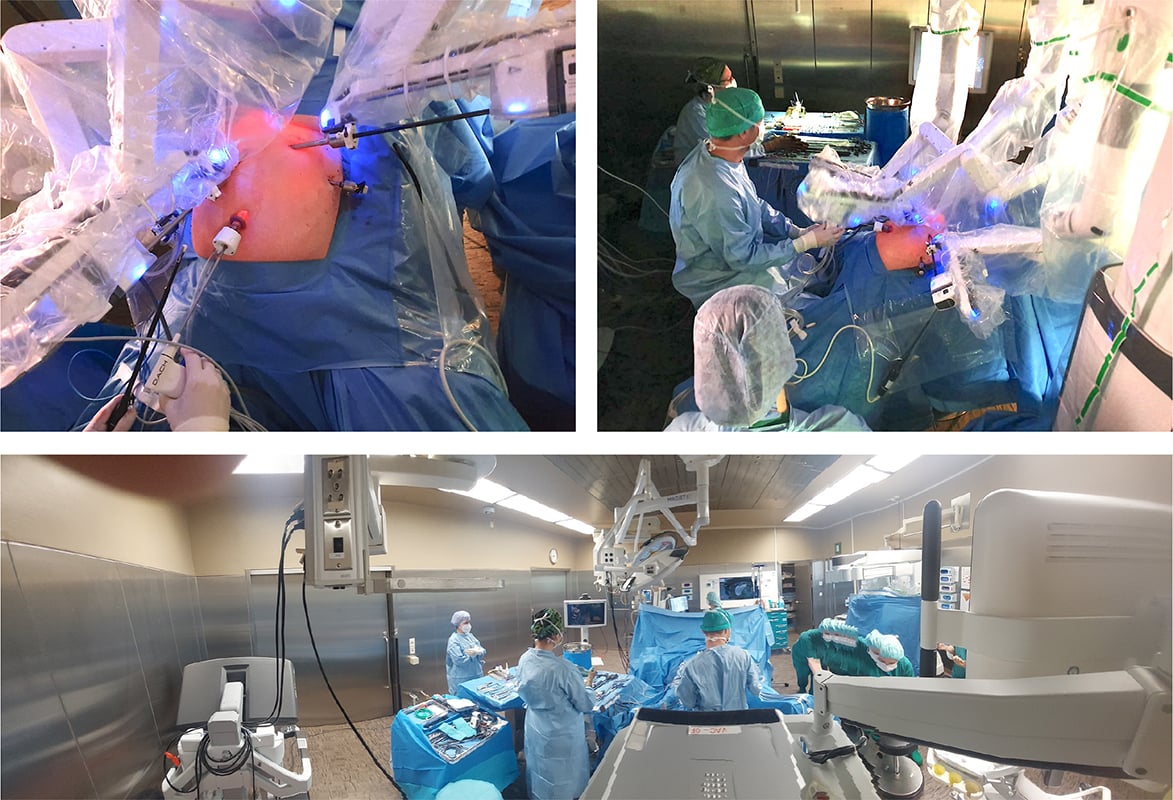
Abb. 1: Robotisch-assistierte Leberresektion. Der Patient ist in French-Position gelagert; der Bedside-Assistent steht zwischen den Beinen; der Operateur sitzt hinter der Konsole; die instrumentierende Pflegekraft steht rechts vom Patienten.
Technische Weiterentwicklungen: Minimalinvasive Leberchirurgie und augmented reality
Die maßgeblichen Neuerungen auf dem Gebiet der minimalinvasiven Leberchirurgie konzentrieren sich auf robotisch-assistierten Eingriffe, welche eine Weiterentwicklung der laparoskopischen Leberchirurgie darstellen. Robotisch-assistierte Leberresektionen werden in Europa und der westlichen Welt in zunehmender Frequenz durchgeführt, mit zunehmender Komplexität der durchgeführten Eingriffe [6].
Den im Vergleich zur laparoskopischen und offenen Leberresektion größten Nachteil stellt jedoch weiterhin die begrenzte Auswahl an Dissektionsverfahren für das Leberparenchym dar. Während inzwischen bei der Laparoskopie alle gängigen Verfahren eingesetzt werden können, sind für die robotische Leberresektion weiterhin nur „Energy devices” verfügbar. Der Harmonic ACE erzeugt hochfrequente mechanische Energie von 55,5 kHz an der aktiven Klinge, um gleichzeitig zu koagulieren und Weichgewebe zu durchtrennen. Eine Abwinkelung des Instrumentes ist jedoch nicht möglich, eigentlich einer der Vorteile des Operationsroboters. Der Vessel Sealer als bipolares Instrument ist abwinkelbar, jedoch aufgrund seiner breiten Klingen in unserer Erfahrung für eine präzise Parenchymdissektion limitiert. Die Renaissance der Clamp-Crush-Technik ist in diesem Zusammenhang als nur als bedingt fortschrittlich zu bezeichnen. Die Einführung eines robotisch zu steuernden Ultraschallaspirator (CUSA), wie er häufig bei der offenen oder laparoskopischen Resektion Einsatz findet, wäre ein wünschenswerter nächster Entwicklungsschritt, um das Indikationsfeld für die robotisch-assistierte Leberchirurgie zu erweitern und noch komplexere Eingriffe zu ermöglichen.
Hinsichtlich der Patientensicherheit und des onkologischen Ergebnisses der robotisch-assistierten Leberchirurgie liegen bis dato keine Daten aus randomisierten kontrollierten Studien vor, es wurden jedoch erste größere Serien und Registerarbeiten zu diesem Thema publiziert [7]. In einer in diesem Jahr in Jama Surgery veröffentlichten großen internationalen Registerarbeit (International Robotic and Laparoscopic Liver Resection study group investigators) wurde die robotische mit der laparoskopischen Hemihepatektomie rechts in 29 internationalen chirurgischen Zentren verglichen [8]. Von 989 Patienten, welche die Einschlusskriterien erfüllten, wurden 220 Patienten robotisch-assistiert und 769 Patienten laparoskopisch operiert. Die robotergestützten Resektionen waren mit einer signifikant niedrigeren Konversionsrate und einem kürzeren postoperativen Krankenhausaufenthalt verbunden. Die Morbidität (Clavien-Dindo > 2) sowie Mortalität (30 und 90 Tage) war in beiden Untersuchungsgruppen gleich verteilt.
In einer im vergangenen Jahr veröffentlichten Metaanalyse von 26 nicht-randomisierten Studien mit 2.630 Patienten (950 roboter-gestützt und 1.680 laparoskopische Leberresektionen) war ebenfalls kein Unterschied in der Komplikationsrate zwischen beiden Verfahren festzustellen [9]. Robotisch-assistierte Leberresektionen waren mit einem signifikant geringeren intraoperativen Blutverlust (Mittelwert: 286 vs. 301 mL, p < 0,001), aber einer längeren Operationszeit (Mittelwert: 281 vs. 221 min, p < 0,001) assoziiert. Befürchtungen hinsichtlich etwaige negativer Effekte auf die onkologischen Radikalität und das Langzeitüberleben nach robotischen Resektionen wurden ausgeräumt, wenngleich diese Erkenntnisse auf retrospektive Analysen beruhen [10–12]. Hier sind prospektive Studien und größere Patientenkollektive notwendig, um diese Fragen abschließend zu klären.
Die Vergütung des Einsatzes eines komplexen Operationsroboters wird weiterhin nicht im DRG-System abgebildet. Da das postoperative (Komplikations-)Management und der verlängerte Krankenhausaufenthalt die wesentlichen Kostentreiber nach offenen Leberresektionen darstellen [13], und diese Kosten durch den Einsatz minimalinvasiver Techniken potenziell reduziert werden, können höhere intraoperativen Kosten durch den Einsatz minimalinvasiver Operationsverfahren prinzipiell amortisiert werden. Aus unserer Sicht wird der Kostendruck auf Seiten der operativen Techniken jedoch weiter fortbestehen und es bleibt abzuwarten, ob es mittelfristig zu einer deutlichen Reduktion der Materialkosten für die robotisch-assistierte Leberchirurgie kommt. Aktuell ist aus unserer Sicht der Einsatz des Operationsroboter bei komplexen Leberresektionen gerechtfertigt, bei kleineren atypischen Resektionen mit kurzer Operationszeit stellt die Laparoskopie weiterhin das Verfahren der Wahl dar [14].
Interessanterweise hat die amerikanische Food and Drug Association (FDA) im Juni dieses Jahres erstmal den Einsatz eines Augmented-Reality-Systems zur Unterstützung im Operationssaal genehmigt (VisAR-Technologie von Novarad, Provo, UT, USA). Dieses System erlaubt, ein 3D-Hologramm basierend auf präoperativ erhobenen bildgebenden Daten über den Körper des Patienten zu projizieren, um so eine Echtzeitführung während Eingriffen an der Wirbelsäule, am Kopf oder am Hals zu ermöglichen. Der Einsatz dieses Systems ist bisher nicht für die Leber vorgesehen, birgt jedoch enormes Potential [15].
Studien im Fokus
Randomisierte kontrollierte Studien, sogenannte RCTs, stellen die Voraussetzung für die Implementierung neuer Entwicklungen in die klinische Praxis und die Verankerung in medizinischen Leitlinien dar. Im vergangenen Jahr und den ersten sechs Monaten dieses Jahres sind die Ergebnisse zahlreicher spannender, auf Leber-chirurgische Fragestellungen fokussierte klinische Studien publiziert worden, welche hier in einer kurzen Auswahl präsentiert werden sollen.
Huang et al. verglichen in einer randomisierten Studie mit insgesamt 344 Patienten mit Hepatozellulärem Karzinom den Effekt von 15 vs. 25 Minuten intermittierendem Pringle-Manöver, mit einer je fünfminütigen Reperfusionsphase [16]. Die verlängerte hiläre Okklusionphase erlaubte eine signifikant schnellere Parenchymdissektion mit geringerem Blutverlust bei gleichzeitig nicht nachweisbarem Effekt auf das postoperative Transaminasenniveau als Parameter für eine möglichen Leberparenchymschädigung, dem primären Endpunkt dieser Studie. Auch in der Subgruppenanalysen von Patienten mit laparoskopisch vs. offener Leberresektionen zeigte sich diesbezüglich kein Unterschied. Obgleich die Studie durch den Einschluss von Patienten mit zumeist Hepatitis B-bedingter Fibrose bzw. Child A-Zirrhose und die Fokussierung auf eine Entität limitiert ist, stellt diese Arbeit einen interessanten Anstoß dar, die Pringle-Zeit zu überdenken und diese Aussagen ggf. in einer multizentrischen Studie weiter zu überprüfen.
Die Applikation von Glucocorticoiden ist Gegenstand zweier weiterer, kürzlich publizierten Arbeiten dar: Steinthorsdottir et al. untersuchten in einer randomisierten, doppelt-verblindeten Studie in Dänemark, ob die einmalige präoperative Gabe von 10 mg/kg Methylprednisolon einen Effekt auf die postoperative Komplikationsrate nach offener Leberresektion hat, im Vergleich zu 8 mg Dexamethason als Standard-Protokoll für die antiemetische Therapie [17]. Die gleiche Fragestellung wurde von Bressan et al. untersucht, ebenfalls in einer doppelt-verblindeten Studie, allerdings wurde hier zwischen 500 mg Methylprednisolon i. v. vs. Plazebo vor Leberresektion randomisiert [18]. Die präoperative Applikation von 10 mg/kg Methylprednisolon führte zu keinem relevanten Effekt auf die Rate an frühen oder späten postoperativen Komplikationen, wenngleich in der untersuchten Kohorte nur ein Viertel der Patienten eine Major-Resektion erhielten.
In die zweite genannte Studie zur präoperativen Applikation von 500 mg Methylprednisolon wurden 151 Patienten eingeschlossen, die ausschließlich eine Major-Resektion erhielten. Die Hauptindikation zur Leberresektion stellte bei 69 % dieser Patienten kolorektale Lebermetastasen dar. Die intraoperative Methylprednisolon-Gabe führte zu einer signifikant niedrigeren Komplikationsrate (31 % vs. 47 %). Eine Einteilung nach der Clavien-Dindo Klassifikation wurde jedoch nicht vorgenommen, weshalb keine differenzierte Aussage über die beobachteten Komplikationen möglich ist. In der Glukokortikoid-Gruppe fanden die Autoren darüber hinaus eine signifikant niedrigere Rate an tiefen Wundinfektionen, wenngleich die Kontrollgruppe im Vergleich zur bekannten Literatur eine insgesamt recht hohe Rate aufwies [19, 20]. Zudem lassen diese Ergebnisse keinen Rückschluss auf Minor-Resektionen zu.
Letztes Jahr wurden zudem die onkologischen Langzeitdaten der OSLO-COMET Studie veröffentlicht, in welcher die laparoskopische mit der offenen Leberresektion zur Therapie kolorektaler Lebermetastasen verglichen wurde. Im Rahmen dieser Studie wurden 280 Patienten randomisiert, primärer Endpunkt war die 30-Tage Morbidität [21]. Eingeschlossen wurden Patienten mit Resektion von kleiner/gleich 3 Lebersegmenten, Ausschlusskriterien waren eine Hemihepatektomie, Gefäß- oder Gallengangsresektion, oder eine Kombination mit interventionellen Verfahren. Diese Arbeit zeigte keine signifikanten Unterschiede im 5-Jahres-Überleben (54 % in der laparoskopischen vs. 55 % in der offenen Gruppe). Da das Langzeitüberleben jedoch nicht den primären Endpunkt dieser Studie darstellt und das Design der Studie für diese Aussage dementsprechend nicht gepowered war, ist die Aussagekraft dieses Ergebnisses limitiert – kann jedoch Anstoß für zukünftige Untersuchungen sein.
Hypertrophieinduktion
Zur Hypertrophieinduktion vor (erweiterter) Leberresektion stehen die portalvenöse Embolisation (PVE) der rechten Pfortader und der in-situ Split (engl. Associating Liver Partition with Portal vein ligation for Staged hepatectomy, ALPPS) zur Verfügung und unterliegen einem fortlaufenden wissenschaftlichen Diskurs. Vorteile der PVE sind die hohe Patientensicherheit und das interventionelle Vorgehen [22]. Dem gegenüber steht ein relativ langes Zeitintervall von vier Wochen bis zur Leberresektion. Ein möglicher Progress der onkologischen Grunderkrankung, welcher in bis zu 30 % der Fälle beschrieben und zu einem Inoperabilität in bis zu 15 % der Patienten [23] führen kann, stellt einen möglichen Nachteil dieses Verfahrens dar.
ALPPS als chirurgisches Verfahren zur Leberaugmentation erfordert ein deutlich kürzeres Hypertrophie-Intervall von nur in der Regel sechs bis acht Tagen, jedoch sind ist eine deutlich höhere Rate an Major-Komplikationen mit 38 % beschrieben im Vergleich zur PVE mit rund 5 % [22]. Dies ist vor allem für Patienten mit einem höheren Risikoprofil relevant, und für Patienten, die sich mutmaßlich mehreren chirurgischen Eingriffen unterziehen müssen, wie beispielsweise bei kolorektalen Tumoren. Eine verbesserte Hypertrophie nach PVE kann möglicherweise durch eine Kombination mit einer Embolisation der rechten und mittleren Lebervene erreicht werden. Dieses Verfahren wurde kürzlich in einer retrospektiven Arbeit aus einer Arbeitsgruppe aus Bordeaux in Frankreich vorgestellt [24]. Vier Wochen nach diesem Eingriff hatte das Lebervolumen um 61 % zugenommen, vs. 29 % in der Gruppe mit alleiniger PVE (p < 0,0001). Diese Fragestellung wird in einer aktuell laufenden RCT (HYPER-LIV01) der gleichen Arbeitsgruppe validiert [24, 25]. Anzumerken ist, dass die Embolisation nicht nur der rechten, sondern auch der mittleren Lebervene eine bessere Hypertrophie begründen kann, da über die klassische PVE das Segment IV nicht adressiert wird [26].
In Zusammenfassung ist die Leberchirurgie durch eine fortwährende Weiterentwicklung sowohl technischer Aspekte als auch des perioperativen Managements geprägt, mit dem Ziel, das operative Vorgehen und das Ergebnis für den Patienten konsequent zu verbessern.
Die Literaturliste erhalten Sie auf Anfrage via [email protected].

Korrespondierender Autor:
Prof. Dr. med. Johann Pratschke
Ärztliche Centrumsleitung Charité Centrum Chirurgie
Direktor der Chirurgischen Klinik
Campus Charité Mitte | Campus Virchow-Klinikum
Charité – Universitätsmedizin Berlin
Augustenburger Platz 1
13353, Berlin, Deutschland

PD Dr. med. Felix Krenzien
Schwerpunkt Leberchirurgie
Chirurgische Klinik, Campus Charité Mitte
Campus Virchow-Klinikum, Charité – Universitätsmedizin Berlin

PD Dr. med. Nathanael Raschzok
Schwerpunkt Leberchirurgie
Chirurgische Klinik, Campus Charité Mitte
Campus Virchow-Klinikum, Charité – Universitätsmedizin Berlin
Chirurgie
Krenzien F, Raschzok N, Pratschke J: Update Leberchirurgie. Passion Chirurgie. 2022 Juli/August; 12(107/08): Artikel 03_03.
Diesen Artikel finden Sie auf BDC|Online (www.bdc.de) unter der Rubrik Wissen | Fachgebiete | Viszeralchirurgie.
Weitere Artikel zum Thema
20.01.2016 Schau Dich schlau
Schau Dich schlau: Nervenschonende offene Rektumresektion
Jetzt neu: Exklusiv für BDC-Mitglieder erscheinen im eMagazin der Passion
01.10.2015 Allgemeinchirurgie
Ungewöhnliche chirurgische Komplikation einer Askaridiasis
Die Askaradiasis spielt in Deutschland aufgrund des hier gegebenen Hygienestandards
Lesen Sie PASSION CHIRURGIE!
Die Monatsausgaben der Mitgliederzeitschrift können Sie als eMagazin online lesen.






















